Ацетон, основные особенности и сферы применения
Компания «Химсервис» предлагает купить ацетон по доступным ценам
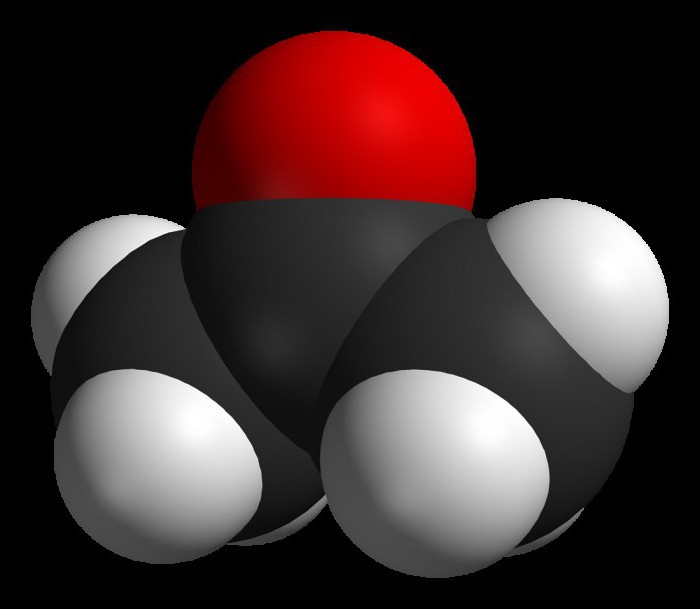
Из школьного учебника химии известно, что самым простейшим органическим соединением, относящимся к группе кетонов, является диметилкетон. Это вещество, единственное из всей группы данных карбонилсодержащих соединений, имеет свое собственное нарицательное название – ацетон. Причем, само слово «кетон» как раз и произошло от немецкого «aketon». Дело в том, что ацетон был получен немецким химиком Андреасом Либавиусом в процессе сухой перегонки ацетата свинца еще в XVI веке, когда не существовало ни единой химической терминологии, ни даже периодической системы элементов.
Ацетон представляет собой бесцветное летучее вещество, обладающее характерным, довольно приятным запахом. Он отличается высокой гигроскопичностью, легко смешивается с водой, метанолом, этанолом, диэтиловым спиртом и другими растворителями в самых произвольных пропорциях.
Основные физические свойства
- Плотность – 0,7899 г/см 3 ;
- Температура кипения – 56,1°С;
- Температура плавления – -95°С;
- Показатель оптического преломления – 1,3591 (при 20°С);
Основные химические свойства
- Молекулярная формула СН3-СО-СН3;
- Относительная молекулярная масса 58,08 г/моль;
Главной химической особенностью ацетона является его высокая реакционная способность. В частности, он является одним из немногих кетонов, способных образовывать бисульфидные соединения. Кроме того, атомы водорода в ацетоне легко замещаются галогенами.
Основные биологические свойства
Ацетон естественным способом вырабатывается в организме всех млекопитающих, включая человека. Он является продуктом метаболических реакций. У здорового человека в крови содержится 1-2 грамма ацетона на 100 мл, кроме того, 0,01-0,03 грамма выделяется в суточном объеме мочи. Повышение содержания ацетона в организме может свидетельствовать о серьезных заболеваниях, в частности, сахарном диабете. Следует упомянуть, что из-за приятного запаха и специфического влияния на нервную систему ацетон можно причислить к наркотическим веществам. Токсикоманы используют его для достижения состояния эйфории.
Однако ацетон в дозах свыше 60 мл смертельно опасен и приводит к существенным негативным изменениям в организме, вплоть до отека легких, пневмонии, гепатита, поражения почек и так далее.
Получение ацетона
Во всем мире производится около 7 миллионов тонн ацетона в год, и этот показатель непрерывно растет. Вплоть до 1914 года данное вещество получали исключительно путем коксования древесины, однако повышенной спрос на ацетон в первой половине XX века привел к появлению более прогрессивных методов. Сегодня основная часть ацетона в мире получается из пропена, например, кумольным методом в три стадии:
В небольших количествах ацетон также получается при брожении крахмала.
Ацетон является важнейшим представителем кетонов и применяется в самых различных областях человеческой жизнедеятельности.
Применение ацетона в промышленности
Ацетон – это самый востребованный в мире растворитель органических веществ, поэтому он в данном качестве широко применяется при производстве различных лаков, клеев, взрывчатых веществ, лекарственных препаратов, строительных очистительных жидкостей и так далее.
Важным преимуществом ацетона является его высокая безопасность по сравнению с альтернативными веществами – скипидаром, керосином или уайт-спиритом. В лабораторных условиях ацетон широко используется для мытья и быстрой сушки химической посуды, окисления различных спиртов, приготовления охлаждающих бань, а также в качестве полярного апротонного растворителя.
Бытовое применение ацетона
Ацетон наверняка имеется практически в каждом доме. Дело в том, что он, обладая весьма доступной стоимостью, является верным помощником в домашнем хозяйстве. В частности, ацетон можно использовать в следующих целях:
- Очистка сложных загрязнений. Ацетон успешно используется для выведения пятен краски с одежды и других объектов. С помощью него можно удалить даже суперклей с тканевой поверхности или остатки застывшего силикона без повреждения базовой структуры материала.
- Обезжиривание различных поверхностей перед покраской или другими работами. Например, металлические изделия перед нанесением слоя лака необходимо тщательно протереть тканью, смоченной в ацетоне.
- Улучшение характеристик бензиновых двигателей. Опытные автолюбители добавляют немного ацетона в бензобак, используя его некоторые важные достоинства. Высокая гигроскопичность позволяет ацетону хорошо перемешиваться с бензином, а качества растворителя помогают удалить накопившийся в форсунках и свечах нагар, а также весь конденсат без вреда для самой системы. Кроме того, из-за высокой концентрации кислорода в ацетоне улучшается воспламенение и сгорание топливной смеси, что снижает расход бензина и увеличивает динамические качества автомобиля.
Меры предосторожности при работе с ацетоном
Несмотря на низкую степень токсичности (в малых объемах), ацетон способен при высоких концентрациях вызывать раздражение кожных покровов и жжение в глазах. Поэтому желательно при длительной работе с веществом использовать средства защиты (респиратор, перчатки и т. д.). Также существенная опасность ацетона заключается в его высокой воспламеняемости (при температуре от +465°С) и взрывоопасности (при концентрации в воздухе от 2,5 до 12%).
Ацетон

Ацетон
Ацетон выпускается по ГОСТ 2768-84
Назначение ацетона
Для применения в качестве растворителя в различных областях промышленности
Состав ацетона
Ацетон технический ГОСТ 2768-84 изготовлен окислением изопропилового спирта.
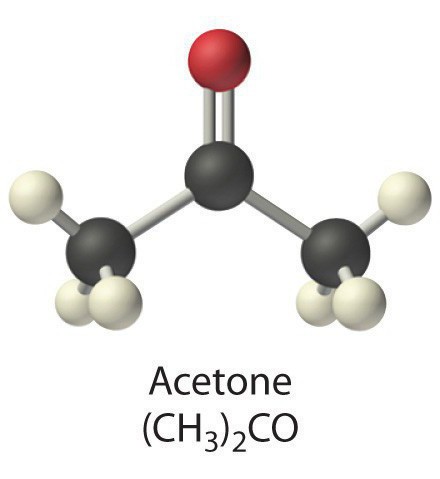
Ацетон (диметилкетон, систематическое наименование: пропанон-2) — простейший представитель кетонов. Формула: CH 3 -C(O)-CH 3 . Бесцветная легкоподвижная летучая жидкость с характерным запахом. Полностью смешивается с водой и большинством органических растворителей. Отличается высокой летучестью.
Свойства ацетона
Ацетон хорошо растворяет многие органические вещества (ацетилцеллюлозу и нитроцеллюлозу, жиры, воск, резину и др.), а также ряд солей (хлорид кальция, иодид калия). Используется для синтеза уксусного ангидрида, ацетонциангидрина, дифенилолпропана и других органических продуктов.
Технические характеристики ацетона
Цветовые решения ацетона
Ацетон представляет собой бесцветную прозрачную жидкость.
Хранение ацетона
Технический ацетон хранят в стальных, алюминиевых, оцинкованных емкостях или бочках и в стеклянных бутылях в соответствии с правилами хранения огнеопасных веществ.
Срок хранения (годности) – 3 месяца.
Фасовка
Технический ацетон заливают в специально выделенные для ацетона железнодорожные цистерны с верхним сливом или универсальным сливным прибором, автоцистерны, в бочки алюминиевые, стальные или оцинкованные, вместимостью от 100 до 275 дм 3 , в стеклянные бутыли по ОСТ 6-09-185, вместимостью 10 и 20 дм 3 . Ацетон, предназначенный для розничной торговли, упаковывают в стеклянные бутыли и флаконы вместимостью 30, 50, 100, 500 и 1000 см 3 3.
Категории
Применение ацетона
Технический ацетон используется для синтеза уксусного ангидрида, ацетонциангидрина, дифенилолпропана и других органических продуктов, а также в качестве растворителя в различных отраслях промышленности.
Меры предосторожности:
По степени воздействия на организм ацетон относится к 4-му классу опасности.
При продолжительном вдыхании паров ацетон накапливается в организме, может всасываться через неповрежденную кожу. Отравление ацетоном возможно при вдыхании паров ацетона в концентрации, превышающей предельно допустимую концентрацию (200 мг/м 3 3).
Ацетон – легковоспламеняющаяся жидкость. При контакте с перекисью натрия или хромовым ангидридом ацетон загорается со взрывом. Все работы с ацетоном должны проводиться с использованием приточно-вытяжной вентиляции вдали от огня и источников искрообразования. В производственных условиях должна быть соблюдена герметизация оборудования, аппаратов, процессов слива и налива для исключения попадания паров ацетона в воздушную среду помещений.
При сливо-наливных операциях необходимо соблюдать правила защиты от статического электричества в производствах химической, нефтехимической и нефтеперерабатывающей промышленности.
В процессе транспортных и производственных операций с ацетоном применяются индивидуальные средства защиты (спецодежда, спецобувь, средства защиты органов дыхания).
Ацетон: формула, особенности свойств, применение
Что собой представляет ацетон? Формула этого кетона рассматривается в школьном курсе химии. Но далеко не все имеют представление о том, как опасен запах данного соединения и какими свойствами обладает это органическое вещество.

Особенности ацетона
Ацетон технический является самым распространенным растворителем, применяемым в современном строительстве. Так как данное соединение имеет невысокий уровень токсичности, его также применяют в фармацевтической и пищевой промышленности.
Ацетон технический используется в качестве химического сырья при производстве многочисленных органических соединений.
Медики считают его наркотическим веществом. При вдыхании концентрированных паров ацетона возможно серьезное отравление и поражение центральной нервной системы. Данное соединение представляет серьезную угрозу для подрастающего поколения. Токсикоманы, которые используют пары ацетона для того, чтобы вызвать состоянием эйфории, сильно рискуют. Медики опасаются не только за физическое здоровье детей, но и за их психическое состояние.
Смертельной считается доза от 60 мл. При попадании в организм значительного количества кетона наступает потеря сознания, а через 8-12 часов – смерть.

Физические свойства
Данное соединение при нормальных условиях находится в жидком состоянии, не имеет цвета, обладает специфическим запахом. Ацетон, формула которого имеет вид СН3СНОСН3, обладает гигроскопическими свойствами. Данное соединение в неограниченных количествах смешивается с водой, этиловым спиртом, метанолом, хлороформом. У него невысокая температура плавления.
Особенности использования
В настоящее время область применения ацетона достаточно широка. Его по праву считают одним из самых востребованных продуктов, применяемых при создании и производстве лакокрасочных материалов, в отделочных работах, химической промышленности, строительстве. Все в большем количестве ацетон применяют для обезжиривания меха и шерсти, удаления из смазочных масел воска. Именно этим органическим веществом пользуются маляры и штукатуры в своей профессиональной деятельности.
Как сохранить ацетон, формула которого СН3СОСН3? Для того чтобы защитить это летучее вещество от негативного воздействия ультрафиолетовых лучей, его помещают в пластиковые, стеклянные, металлические флаконы подальше от УФ.
Помещение, где предполагается размещение существенного количества ацетона, необходимо систематически проветривать и установить качественную вентиляцию.

Особенности химических свойств
Название данное соединение получило от латинского слова «ацетум», означающее в переводе «уксус». Дело в том, что химическая формула ацетона C3H6O появилась гораздо позже, чем было синтезировано само вещество. Его получали из ацетатов, а затем использовали для изготовления ледяной синтетической уксусной кислоты.
Первооткрывателем соединения считают Андреаса Либавиуса. В конце XVI века путем сухой перегонки ацетата свинца ему удалось получить вещество, химический состав которого был расшифрован только в 30-х годах XIX века.
Ацетон, формула которого СН3СОСН3, до начала XX века получали путем коксования древесины. После повышения спроса во время Первой мировой войны на это органическое соединение, стали появляться новые способы синтеза.
Ацетон (ГОСТ 2768-84) является технической жидкостью. По химической активности данное соединение является одним из самых реакционноспособных в классе кетонов. Под воздействием щелочей наблюдается адольная конденсация, в результате которой образуется диацетоновый спирт.
При пиролизе из него получают кетен. В реакции с циановодородом образуется ацетонцианидангидрин. Для пропанона характерно замещение атомов водорода на галогены, происходящее при повышенной температуре (либо в присутствии катализатора).
Способы получения
В настоящее время основное количество кислородсодержащего соединения получают из пропена. Технический ацетон (ГОСТ 2768-84) должен обладать определенными физическими и эксплуатационными характеристиками.
Кумольный способ состоит из трех стадий и предполагает производство ацетона из бензола. Сначала путем его алкилирования с пропеном получают кумол, затем окисляют полученный продукт до гидропероксида и расщепляют его под воздействием серной кислоты до ацетона и фенола.
Кроме того, это карбонильное соединение получают при каталитическом окислении изопропанола при температуре около 600 градусов по Цельсия. В качестве ускорителей процесса выступают металлическое серебро, медь, платина, никель.
Среди классических технологий производства ацетона особый интерес представляет реакция прямого окисления пропена. Данный процесс осуществляется при повышенном давлении и присутствии в качестве катализатора хлорида двухвалентного палладия.
Также можно получить ацетон путем брожения крахмала под воздействием бактерий Clostridium acetobutylicum. Кроме кетона среди продуктов реакции будет присутствовать бутанол. Среди недостатков этого варианта получения ацетона отметим несущественный процентный выход.
Заключение
Пропанон является типичным представителем карбонильных соединений. Потребители знакомы с ним как с растворителем и обезжиривателем. Он незаменим при изготовлении лаков, лекарственных препаратов, взрывчатых веществ. Именно ацетон входит в состав клея для кинопленки, является средством для очистки поверхностей от монтажной пены и суперклея, средством промывки инжекторных двигателей и способом повышения октанового числа горючего, и т.п.
Kotsant › Блог › про Ацетон!

Для начала немного теории.
Ацетон — (диметилкето́н, систематическое наименование: пропано́н) — простейший представитель кетонов. Формула: CH3-C(O)-CH3. Бесцветная легкоподвижная летучая жидкость с характерным запахом. При 20°C растворимость газа О2: 3,1 мл на 100 мл воды, 22 мл на 100 мл этанола, 23,1 мл на 100 мл ацетона. Полностью смешивается с водой и большинством органических растворителей. Ацетон хорошо растворяет многие органические вещества (ацетилцеллюлозу и нитроцеллюлозу, воск, резину и др.), а также ряд солей (хлорид кальция, иодид калия).
Жирным я выделил то на чем хотелось бы заострить внимание.
1. Это концентрация кислорода в ацетоне. Она наивысшая из недорогих добавок (в том же оксиде натрия NO2 его в десятки раз больше).
Повышение содержание молекул кислорода в бензине — это хорошо. Смесь будет лучше перемешиваться перед поджогом, за счет сильной летучести ацетона и будет сгорать полностью за счет скорости горения кислорода.
Мы получим более экономичное авто и чуть больше крутящего момента из-за сильного расширения ацетона при нагреве в камере сгорания.
Кстати, ацетон и так добавляют в высокооктановый бензин, но в целях экономии — немного.
При нормальной работе всех датчиков (температура выхлопа, лямбда-зонд) мозги машины прекрасно корректируют смесь под “новое” топливо.
Особенно ацетон актуален в летнее время. В зимнее слухи о том что с ним машина лучше заводится — неоднозначные т.к. из уроков химии мы могли помнить что при -20 ацетон замерзает.
Температура-же самовоспламенения ацетона — +465 °C
По сравнению с бензином 257 °C (без присадок).
Учитывая этот факт мы видим улучшенную детонационную стойкость ацетона — меньше риск что он загорится раньше чем заискрит свеча, например просто от жара в цилиндре.
2. Ацетон полностью смешивается с водой удаляя из системы автомобиля весь конденсат, сжигая его в камере сгорания и выкидывая его на улицу через трубу )))
Все знаю что влага внутри бензобака это вредно для насоса и всего остального. Ацетон смешиваясь с водой позволяет пройти воде далее к двигателю . Без ацетона вода скапливается в низинах т.к. бензин легче воды и она опускается вниз. Ну налейте в стакан с водой немного бенза — поймете. 🙂
3. Ацетон растворяет всякое разное гумно. Это гумно нагарает на свечах и форсунках. По сравнению с использованием спец. чистящих средств, ацетон более мягко отчищает элементы двигателя и на нем можно ездить каждый день, а не ставить машину на сервис для чистки. Он всегда присутствует в системе не давая образоваться новому налету гумна.
4. Ацетон отлично смешивается с самим бензином из-за схожей плотности (Плотность бензина = 0,75 г/см³, плотность ацетона = 0,78 г/см³).
5. Безопасность для двигателя.
Температура горения ацетона в 10 раз ниже чем у бензина, что благотворно сказывается на работе самого двигателя при высоких нагрузках.
Плюсы ацетона в бензе:
Меньше риск детонации (повышения октанового числа)
Удаление гумна на свечах и форсунках
Удаление воды из системы
Понижение расхода
Более ровная работа на холостых
Повышается тяга на низах
Минусы
Выглядишь как мудак на заправке.
Быстро подсаживаешься на эту хрень и кажется что без ацетона тачка уже не едет.
Кроме заправки тратишь время на поход в магазин хозтоваров.
В магазине, если покупать в одном и том-же, продавцы начинают искать в вас признаки наркобарыги.
Далее я расскажу о Применении.
Дозировка.
Я лью на полный бак 300-350 мл.
При единичной заправке на 15 литров я сначала плескаю 70-100 мл ацетона. Потом лью бенз чтобы лучше перемешалось.
Покупка.
Покупаем чистый технический ацетон без присадок и добавок. Тупо ацетон.
Стоит рублей 70 бутылка 500 мл.
Вроде все рассказал.
Статья принадлежит мне! © Роман Гришин. :))) woltswagin
Что сильнее – ацетон или растворитель

Из этой статьи вы узнаете:
- Что такое ацетон
- Где его используют
- Какие виды растворителей бывают
- Что сильнее – ацетон или растворитель
- Как работать с ацетоном и другими современными растворителями
Вряд ли сегодня можно встретить человека, который не был бы знаком с каким-либо видом растворителей – они уже давно стали неотъемлемой частью нашего быта. Без них не получится обойтись в случае выполнения каких-либо работ, связанных с покраской. Люди старшего поколения наверняка помнят, что раньше масляную краску разводили ацетоном, его же использовали, если возникала необходимость в удалении старого лакокрасочного покрытия. В этой статье расскажем, что сильнее – ацетон или растворитель, разберемся, в чем заключается разница между ними, расскажем, какие еще бывают растворители и как с ними работать.
Что такое ацетон и где его применяют
Прежде чем ответить на вопрос, что сильнее – ацетон или растворитель, разберемся, что же собой представляет ацетон. Это бесцветная летучая жидкость, имеющая органическую природу и формулу C3H6O. Это простейший из насыщенных кетонов, наиболее распространенный среди всех видов растворителей.
Для ацетона характерно наличие резкого специфического запаха. Среди его особенностей можно отметить легкость при смешивании с водой и органическими растворителями, такими как эфир, этиловый и метиловый спирты. Температура кипения ацетона незначительна – примерно +56,1 °C, температура плавления – +95 °C. Эта жидкость является легковоспламеняемой и высокогорючей.
Рекомендуемые статьи по теме:
Первоначально ацетон получали при перегонке древесины. На сегодняшний день, в связи с масштабностью и актуальностью его производства, используются технологии зернового или мелиссового брожения. Это вещество также может быть получено в результате контроля углеводородного окисления.
Ацетон имеет существенное значение в различных отраслях и процессах. Он используется при:
- растворении лаков, нитролаков, нитроэмалей, ацетилена, нитроцеллюлозы, резины, восков, жиров и прочих веществ;
- удалении лакокрасочных покрытий и лака для ногтей;
- растворении некоторых солей (например, йодистого калия, хлористого кальция и т. п.);
- изготовлении ряда лекарственных препаратов;
- создании искусственного шелка;
- производстве небьющейся органической стеклянной продукции и пластмассы, в основе которой лежит нитрат целлюлозы – целлулоид;
- получении нитропороха (недымящейся взрывчатки);
- изготовлении пленок для киносъемок и т. п.
В связи со способностью ацетона к отличному растворению ацетилена он активно используется при необходимости наполнения стальных баллонов, которые предназначаются для хранения ацетилена. Кроме того, с его помощью можно легко очистить разного рода поверхности и инструменты от монтажной пены.
Ацетон входит в состав многих химических продуктов, без него невозможно создавать парфюмерную продукцию, красители (к примеру, индиго), искусственный каучук и искусственную кожу. Он применяется для эффективного обеззараживания шерсти и мехов. Вместе с солями кислот (сернистой и гидросернистой) используется в процессах покраски и печатания текстильных изделий.

За счет того, что токсичность ацетона умеренная, возможно его применение в фармацевтической, пищевой отраслях производства. Он помогает в экстрагировании ряда лекарственных препаратов, пищевых продуктов, жиров, витаминов.
Другие растворители и сфера их применения
Существующие на сегодняшний день растворители могут быть:
Первая группа пользуется более широким спросом в сравнении со второй. В зависимости от присущих физических особенностей, эту группу можно подразделить на следующие виды растворителей:
- Трудноулетучивающиеся. В эту категорию входит, к примеру, скипидар. Эти растворители используют при работе с эмалями или лаками.
- Среднеулетучивающиеся (например, керосин). Они больше подходят для работы с масляными и акриловыми красителями.
- Легкоулетучивающиеся. К этому разряду можно отнести, к примеру, бензин, уайт-спирит, сольвент. Они находят применение при работе с эмалями, лаками, акриловыми и масляными красителями. Использование этого типа растворителей требует соблюдения предельной осторожности, за счет своей летучести они являются чрезвычайно взрывоопасными.
Большая часть растворителей относится к подвижным жидким субстанциям, отличающимся сильным специфическим запахом, который можно рассматривать в качестве основного недостатка.

Среди неорганических растворителей отметим:
- воду;
- жидкий аммиак;
- серную, фосфорную и пр. соли.
Для органических растворителей характерны существенные недостатки, в число которых входит специфический устойчивый запах, который не выветривается в течение достаточно длительного времени, легкую воспламеняемость, токсичность испарений, которые также могут послужить причиной серьезных отравлений.

Красители, для растворения которых используется вода, пользуются широким спросом за рубежом, в России они гораздо менее востребованы, поскольку быстро теряют свои качества в процессе хранения в суровом российском климате.
Несмотря на наличие большого числа опасных свойств, в нашей стране большим спросом пользуются именно органические растворители. Они могут быть:
- углеводородными;
- спиртовыми;
- сложными эфирами.
Остановимся несколько подробнее на особенностях и свойствах наиболее востребованных из них. Среди углеводородных растворителей можно выделить:
- Уайт-спирит – представляет собой бесцветную маслянистую жидкость. Он отличается чрезвычайной горючестью и запахом, который схож с запахом керосина. Несмотря на относительно невысокие растворяющие показатели, это средство пользуется широким спросом в связи со своей относительной дешевизной и нетоксичностью.
- Нефтяной бензол является бесцветной, быстроиспаряющейся жидкостью, не относящейся к водорастворимым. Как и прочие органические растворители, отличается сильным специфическим запахом. Нефтяной бензол может совмещаться с углеводородными соединениями. Для него характерно выделение токсичных, огнеопасных паров, а также повышенная взрывоопасность при взаимодействии с воздухом.
- Скипидар может быть живичным и пневым. Предпочтительнее использовать первый. Эту бледно-желтую с резким специфическим запахом жидкость применяют при необходимости разведения шпатлевок и масляных лакокрасочных материалов.
- Бензин относится к продуктам нефтепереработки. Для него характерна высокая огнеопасность, быстрота испарения. Определенное количество паров бензина, сконцентрированное в воздухе, может вызвать их детонацию.
Остановимся чуть подробнее на спиртовых растворителях, среди которых выделяются:
- Этиловый спирт – бесцветная жидкость с характерным запахом. Для этого вида растворителя важно отсутствие посторонних примесей. Попадание большой концентрации его паров в дыхательные пути способно стать причиной тяжелейшего отравления. Он отличается возможностью воспламенения не только из-за контакта с огнем или искрой, но и просто от воздействия высокой температуры.
- Бутиловый спирт. Его используют при работе с нитроцеллюлозными лаками. В этом случае покрытие будет отличаться блеском, большей гладкостью, меньшей подверженностью побелению.
- Метиловый спирт (метанол) представляет собой прозрачную, чрезвычайно ядовитую жидкость, в состав которой обычно входят эфиры и ацетон.
- Этилетиленгликоль является прозрачной бесцветной жидкостью, образующей однородное соединение при взаимодействии с водой. Благодаря длительному времени испарения он незаменим в процессе работы с нитролаками. Его применение придает покрытиям блеск, гладкость, простоту последующей полировки.
Что сильнее – ацетон или растворители, включенные в группу сложных эфиров:
- Метилацетат является быстроиспаряющейся подвижной жидкостью с повышенными пожароопасными и ядовитыми свойствами. Температура кипения этого растворителя варьируется в пределах +56…+58 °С.
- Этилацетат – для этого растворителя характерен более длительный период испарения, приятный запах, температура его кипения колеблется в пределах от +77 до +82 °С.
- Бутилацетат – желтоватая жидкость с длительным периодом испарения. За счет этого свойства этим средством пользуются при необходимости увеличить время, требуемое для высыхания покрытия.
- Амилацетат является прозрачной жидкостью с приятным запахом и длительным сроком испарения. По этой причине, как и бутилацетат, его применяют в случае необходимости замедления процесса высыхания.
- Ацетон отличается характерным, резким, неприятным запахом, чрезвычайной летучестью и пожароопасностью.

Для разведения концентрированных нитролаков и придания им необходимой степени вязкости пользуются растворителями, входящими в группу сложных эфиров. Отметим, что на качественные свойства покрытия напрямую влияют элементы состава. К примеру, содержание наибольшего количества быстроиспаряющихся растворителей может привести к помутнению покрытия, однако добавление в состав веществ, которые замедляют период сушки, придаст покрытию блеск, гладкость, незамутненность.
Что сильнее – ацетон или растворитель
Итак, что же сильнее – ацетон или растворитель? Из приведенного выше описания становится понятным, что ацетон относится к одной из разновидностей растворителей. При этом стоит отметить, что какими-либо особыми характеристиками он не обладает. По сути, к растворителям можно отнести любой вещество, которое наделено способностью растворять в себе иные вещества.
Растворители могут иметь жидкую, газообразную и даже твердую форму. Мы не будем перечислять все их названия, поскольку таких слишком много. В общем-то, и обычная вода является растворителем, при этом достаточно эффективным. Это можно подтвердить на примерах чая или кофе с сахаром – в воде быстро растворяются и сахар, и те вещества, что присутствуют в чайном листе и кофейных зернах.
Однако вода относится к естественным, природным растворителям, в то врем как ацетон впервые стал известен в 1595 году. Он был получен немецким химиком Андреасом Либавиусом, который занимался сухой перегонкой ацетата свинца. Впрочем, название ацетону было дано лишь в 1848 году соотечественником Либавиуса Леопольдом Гмелином, именно он ввел в обиход это название. Говорить о том, что сильнее – ацетон или растворитель, не совсем корректно, поскольку первый является конкретным химическим соединением, в то время как второй представляет собой большой класс разнообразных химических веществ и соединений.
Точную химическую формулу ацетона вывели чуть раньше – в 1832 году. Открыта она была немцем Юстусом фон Либихом и французом Жаном-Батистом Дюма. До начала Первой мировой войны для производства ацетона использовали исключительно метод коксования древесины, однако с увеличением спроса на этот растворитель стал актуальным поиск более эффективных способов производства, что в конечном итоге и было выполнено. На этом примере отчетливо видно, как военная необходимость приводит к научно-техническому прогрессу.
Итак, что же сильнее – ацетон или растворитель? Приведенная ниже таблица покажет, в чем заключаются основные отличия между ними.
Ацетон
Растворитель
Что собой представляет
В обычных условиях является жидкостью, температура кипения которой составляет +56,1 °С. Химическая формула CH3–C(O)–CH3
Многочисленный класс, представленный самыми разнообразными соединениями
В основном, в качестве растворителя, кроме того используется в качестве сырья при производстве ряда химических соединений и как добавка в ацетилен для его безопасного хранения
Как растворитель во всех областях человеческой деятельности
Как работать с ацетоном и другими растворителями
Независимо от того, что сильнее – ацетон или растворитель, работа с любым из них требует соблюдения техники безопасности. Очень важно обеспечение защиты, в первую очередь, трех стратегически важных участков тела, а также органов:
- Рук, поскольку именно за их счет осуществляется контакт с ацетоном или растворителем, неправильное обращение может стать причиной химического ожога.
- Рта, носа, являющихся органами дыхания, так как чрезмерное вдыхание паров растворителя грозит возникновением химического отравления.
- Глаз, защищаемых от попадания капель и брызг от ацетона или растворителя.
В связи с этим большое значение при работе имеет выбор правильной одежды, способной максимально снизить вероятность причинения вреда растворителем организму человека. Неважно, что сильнее – ацетон или растворитель, работая с любым из них, нужно надевать фартук, прятать волосы под шапочку, защищать руки перчатками, для носа и рта использовать респиратор, а для защиты глаз – специальные очки.

Использование перчаток в процессе работы с растворителями позволит избежать контакта этого вещества с кожей. Для перчаток важна полная водонепроницаемость, то есть для их изготовления должна использоваться не ткань, а преимущественно плотная резина или латекс. Нельзя пользоваться тонкими резиновыми перчатками, поскольку при работе с органическими растворителями они могут просто расплавиться.
В связи с высокой степенью опасности для человека испарений химикатов из первой группы растворителей при работе с ними существенное значение имеет защита органов дыхания посредством обычного респиратора.
Во избежание попадания растворителя в глаза необходимо использование специальных защитных очков, приобрести которые можно, обратившись в любой специализированный строительный магазин.
Неважно, что сильнее – ацетон или растворитель, работа с ними требует определенной подготовки. В первую очередь оценивается как опасность самого вещества, так и объем предстоящей работы. Так, при необходимости удаления с плитки маленького пятнышка можно использовать обычный бензин, усиленные меры предосторожности при этом вам не потребуются (главное, не забыть про перчатки). Но если вы собираетесь работать с растворителями в течение нескольких часов в небольшом помещении, то в обязательном порядке воспользуйтесь всеми перечисленными выше защитными средствами.
Независимо от того, что сильнее – ацетон или растворитель, работа с этими средствами требует соблюдения следующих правил:
- Бутылка или банка со средством должна стоять на видном месте, лучше перед вами, но при этом слегка в стороне от используемых инструментов и других средств.
- Держите при себе влажную тряпку, которую используйте для протирания поверхностей при попадании на них капель растворителя.
- Работа с растворителями требует максимальной внимательности.
- Не имеет значения, что сильнее – ацетон или растворитель, их использование должно осуществляться исключительно в соответствии с назначением, четким соблюдением дозировки, указанной в инструкции к составам.
По окончании работы с растворителями все емкости должны быть максимально плотно закрыты, использованная посуда тщательно вымыта или выброшена. А для удаления резкого химического запаха из помещения его достаточно просто как следует проветрить.
Где купить ацетон и другие современные растворители
АО «Радуга» работает с 1991 года (бывшие «Центрмебелькомплект», «Декор-1»). Фирма была организована для снабжения сырьем предприятий, входящих в состав ЗАО «Центромебель».

Сегодня постоянными деловыми партнерами компании являются не только российские производители, но и ведущие фирмы Германии, Австрии, Франции, Италии, Швейцарии, Финляндии, Польши, Швеции. В центре Москвы расположен наш офис, а также собственный складской комплекс с выставочным залом площадью 200 м².
На наших складах, расположенных в ближнем Подмосковье, всегда в наличии большой выбор сырья, материалов и комплектующих для производства мебели и столярных изделий. В ассортименте более 300 наименований лаков и 400 наименований красителей, сделан упор на продажу лаков и красителей с сухим остатком.
По заявкам покупателей наша команда за один-два дня изготавливает полиуретановые эмали практически всех цветов. Мы предлагаем клеи от пяти ведущих производителей Европы, шпон натуральный и пиломатериалы – более 60 наименований обычных, экзотических и эксклюзивных пород. В наличии постоянно имеется лицевая и крепежная фурнитура – более 4000 наименований от изготовителей из Европы: Австрии, Польши, Германии и т.д.
Каждый месяц мы обрабатываем заявки более 1800 клиентов. В их число входят как крупные мебельные фабрики, так и частные предприниматели.
Поставки товара осуществляются по всей России. Наша компания бесплатно доставляет товары по Москве. Продукция отправляется автомобильным транспортом по всем регионам России.
Наша фирма серьезно относится к подготовке собственных специалистов. Менеджеры систематически проходят стажировки в занимающихся производством отделочных материалов фирмах Германии, Италии, Австрии, Финляндии. Работники нашей компании оказывают техническую помощь клиентам.
Приглашаем Вас к сотрудничеству на взаимовыгодных условиях! Мы дорожим своими клиентами и стараемся найти индивидуальный подход к каждому покупателю.
Ацетон
(Диметилкетон)
Ацетон – (от лат. acetum – уксус) (2-пропанон, диметилкетон) СН3СОСН3, молекулярная масса 58,079; летучая бесцветная жидкость с характерным запахом; температура плавления –94,6°С, температура кипения 56,1 °С. широко применяемый растворитель органических веществ, в первую очередь нитратов и ацетатов целлюлозы; благодаря сравнительно малой токсичности он используется также в пищевой и фармацевтической промышленности; ацетон служит также сырьем для синтеза уксусного ангидрида, кетена, диацетонового спирта, окиси, мезитила, метилизобутилкетона, метилметакрилата, дифенилолпропана, изофорона и многих других соединений. Смешивается с водой и органическими растворителями, например эфиром, метанолом. этанолом. сложными эфирами.
Так же он обладает всеми химическими свойствами, характерными для алифатических кетонов. Образует кристаллические соединения с гидросульфитами щелочных металлов. например с NaHSO3 – (CH3)2C(OH)SO3Na. Только сильные окислители. например щелочной раствор КМnО4 и хромовая кислота, окисляют ацетон до уксусной и муравьиной кислот и далее – до СО2 и воды. Каталитически восстанавливается до изопропанола, амальгамами Mg или Zn, а также Zn с СН3СООН – до пинакона (СН3)2С(ОН)С(ОН)(СН3)2. Атомы водорода легко замещаются при галогенировании. нитрозировании и т.п. Действием хлора и щелочи ацетон превращается в хлороформ, который взаимодействует с ацетоном с образованием хлорэтона (СН3)2С(ОН)ССl3, применяемого как антисептик.Технический ацетон получается кумольным методом в процессе синтеза фенола, методом ацетонобутилового брожения, а также в качестве побочного продукта в ряде производств.Ацетон находит применение в лакокрасочной промышленности, используется при производстве пластмасс, синтетического каучука и химических волокон, служит сырьем для синтеза многих других органических продуктов. Он используется в производстве уксусного ангидрида, ацетонциангидрина, дифенилолпропана, для обезжиривания поверхностей, как растворитель в различных отраслях промышленности.
Получение ацетона в промышленности.
Ацетон получают несколькими способами:
Метод Удриса-Сергеева или кумольный способ .
Он осуществляется в три стадии. На первой стадии бензол алкилируют пропиленом до изопропилбензола (кумола), который затем окисляют кислородом в щелочной среде при 130°C до кумилгидропероксида. В результате гидролиза последнего в кислой среде при 60°C образуются конечные продукты процесса – фенол и ацетон:
C6H6 + CH3CH=CH2 –> C6H5CH(CH3)2
C6H5CH(CH3)2 + O2 –> C6H5C(CH3)2OOH
C6H5C(CH3)2OOH –> C6H5OH + (CH3)2C=O
– Окисление изопропилового спирта в паровой фазе при 450-650°C в присутствии металлической меди, серебра, никеля или платины:
(CH3)2CHOH + 1/2O2 –> (CH3)2C=O + H2O
– автокаталитическое окисление изопропанола в жидкой фазе при 90-140°C и 0.2-0.3МПа. Помимо ацетона продуктом процесса является перекись водорода:
(CH3)2CHOH + O2 –> (CH3)2C=O + H2O2
– Прямое окисление пропилена в жидкой фазе в присутствии хлорида палладия PdCl2 при 50-120°C и 5-10МПа:
CH3CH=CH2 + PdCl2 + H2O –> (CH3)2C=O + Pd + 2HCl
Pd + 2HCl + 1/2O2 –> PdCl2 + H2O
Применение
Технический ацетон широко применяется в лакокрасочной промышленности в качестве растворителя нитролаков, нитроэмалей (при выработке авиационных, автомобильных, кабельных, кожевенных и других лаков), при получении ацетилцеллюлозы и нитроцеллюлозы, в производстве некоторых сортов искусственного шёлка, при изготовлении органического небьющегося стекла, в производстве киноплёнок, бездымного пороха, целлулоида, акрихина и других.
Способность ацетона растворять ацетилен используется в широких масштабах при наполнении стальных баллонов, в которых хранится ацетилен, применяемый для сварки металлов. Ацетилен поглощается пористым материалом, пропитанным ацетоном; при давлении 15 атм. 1 объём он растворяет 375 объёмов ацетилена.
Применение ацетона для извлечения воска из смазочных масел приобретает всё большее значение. Ацетон служит сырьём для производства многих химических продуктов: синтетического каучука, индиго, ионона (духи), сульфонала (снотворное средство). Соединения ацетона с солями сернистой и гидросернистой кислот применяют при крашении и печатании тканей.
Технический ацетон находит применение в производстве искусственной кожи, для обеззараживания шерсти и меха, для извлечения эфирных масел. Чистый ацетон применяется в пищевой промышленности при экстрагировании пищевых продуктов, витаминов, жиров; для экстрагирования некоторых лекарств и приготовления фармацевтических препаратов, требующих химически чистого растворителя с низкой температурой кипения.
Также его применяют для обезжиривания поверхностей или изделий используемых в промышленности и в быту. Ацетон широко используется в промышленности как растворитель для извлечения ряда веществ, для перекристаллизации химических соединений, химической чистки, получения хлороформа и т. д. Пары ацетона тяжелее воздуха. Поэтому в помещениях, в которых происходит испарение ацетона, создается опасность отравления при вдыхании его паров, находит применение в лакокрасочной промышленности, используется при производстве пластмасс, синтетического каучука и химических волокон, служит сырьем для синтеза многих других органических продуктов. Он используется в производстве уксусного ангидрида, ацетонциангидрина, дифенилолпропана, для обезжиривания поверхностей, как растворитель в различных отраслях промышленности. Ацетон транспортируют транспортом всех видов в соответствии с правилами перевозок грузов, действующими на транспорте данного вида. Воздушным транспортом перевозят только на грузовых судах с максимальным объемом нетто на одну упаковку 60 дм 3 . По железной дороге перевозят в бочках в крытых вагонах (повагонными или мелкими отправками). При транспортировании ацетона в бочках вместимостью 100 дм 3 в крытых железнодорожных вагонах, речным и морским транспортом перевозку осуществляют пакетами в соответствии с правилами перевозки грузов. Ацетон в бутылях перевозят только автомобильным транспортом.
Обнаружение ацетона
В химико-токсикологическом анализе для обнаружения ацетона применяют реакциис растворами иода, нитропруссида натрия, фурфурола, о -нитробензальдегида и метод микродиффузии.
Реакция образования йодоформа. При взаимодействии ацетона с раствором иода в щелочной среде образуется йодоформ: Выполнение реакции. К 1 мл исследуемого раствора прибавляют 1 мл 10 %-го раствора аммиака и несколько капель раствора иодав иодиде калия. В присутствии ацетона образуется желтый осадок йодоформа с характерным запахом, а его кристаллы имеют характерную форму.
Предел обнаружения: 0,1 мг ацетона в пробе.
Эту реакцию дает и этиловый спирт.
Меры предосторожности
По степени воздействия на организм ацетон относится к 4-му классу опасности. При продолжительном вдыхании паров ацетон накапливается в организме, может всасываться через неповрежденную кожу. Отравление ацетоном возможно при вдыхании паров ацетона в концентрации, превышающей предельно допустимую концентрацию (200 мг/м3).
По фармакологическим свойствам ацетон относится к числу веществ, проявляющих наркотическое действие. Он обладает кумулятивными свойствами. Ацетон медленно выводится из организма. Он может поступать в организм с вдыхаемым воздухом, а также через пищевой канал и кожу. После поступления ацетона в кровь часть его переходит в головной мозг, селезенку, печень, поджелудочную железу, почки, легкие и сердце. Содержание ацетона в указанных органах несколько меньшее, чем в крови. При работе с техническим ацетоном нужно соблюдение следующих мер предосторожности:
– защищать от попадания на кожу рук с помощью резиновых перчаток;
– не допускать попадания на слизистые оболочки глаз;
– работы с применением ацетона проводить в хорошо проветриваемых помещениях, или с использованием защитных дыхательных масок;
При попадании ацетона на кожу, необходимо его быстро смыть большим количеством теплой воды с мылом.
Токсичность ацетона и распространенность отравлений
Ацетон сравнительно мало токсичен. Нелсон и др. нашли, что максимально допустимая концентрация ацетона в воздухе при 8-часовом воздействии составляет 0,02%. Дринкер и Кук считают, что максимально допустимая концентрация ацетона равна 0,05–0,25%. Смит и Майерс приводят случаи острого отравления парами смеси ацетона и бутанона при концентрациях порядка 0,1%. Неопубликованные исследования Штернера, Оглезби и Фассета показали, что из всех растворителей, применяемых в промышленности, ацетон является одним из наименее токсичных и в этом отношении вполне сравним с этиловым спиртом. В настоящее время максимально допустимой концентрацией принято считать 0,1%. Пребывание в течение короткого времени в атмосфере, в которой концентрация ацетона намного превышает указанную, не причиняет вреда.
Пределы воспламенения в воздухе 2,55–12,8 об.%.
Ацетон является естественным метаболитом организма человека и животных. Он входит в триаду соединений (бета-оксибутират, ацетоацетат и ацетон), обозначаемых, как кетоновые тела. Ацетон образуется путем неферментативного декарбоксилирования ацетоуксусной кислоты. В нормальных условиях содержание ацетона в сыворотке крови человека обычно не превышает 6 мг/л (0,1 ммоль/л). Трехдневное голодание приводит к увеличению концентрации ацетона в сыворотке у лиц с ожирением до 17 мг/л, а у здоровых людей, не страдающих ожирением до 44 мг/л
В условиях дефицита глюкозы (голодание) или при снижении ее биодоступности (сахарный диабет), содержание кетоновых тел в крови может возрастать в десятки раз. При этом они действуют и как часть регуляторного механизма с обратной связью, блокируя чрезмерную мобилизацию жирных кислот из жировой ткани и ослабляя тем самым токсическое действие последних.
Токсичность ацетона, поступающего в организм извне хорошо изучена. Острая токсичность ацетона (LD50), поступающего через желудок составляет по данным разных авторов для крыс – 5,8–9,8 г/кг, для мышей – 3,0–5,25 г./кг, для кроликов и собак – 3,8–8,0 г/кг. По этому показателю ацетон мало отличается от этанола.
Эффективная однократная действующая доза (EDmin) ацетона для человека, определяемая по его влиянию на нервную систему, почки и кровь при условии поступления через желудок, составляет 2,9 г/кг.
Доза, обладающая минимальным токсическим действием (ПДхр.), определяемая на крысах при условии внутрижелудочного введения ацетона на протяжении 6 мес. составляет 7 мг/кг.
Его предельно допустимая концентрация (ПДК) в воде общего пользования составляет 2,2 мг/л.
Токсическое действие ацетона связано с наркотическим влиянием на ЦНС, прижигающим действием на слизистую оболочку дыхательных путей и органов пищеварения, метаболическим ацидозом и негативным влиянием на развитие плода.
Не нашли что искали? Вы можете оставить заявку, в форме обратной связи.


